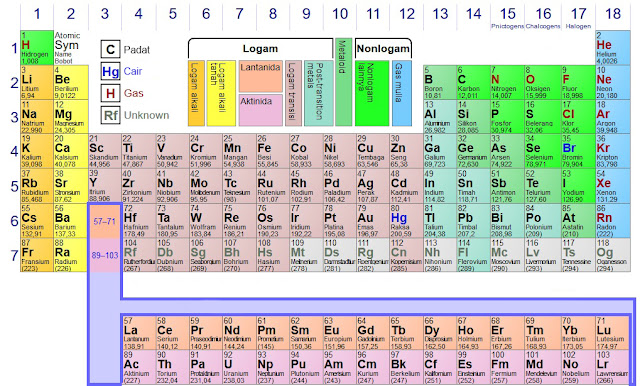
Menurut Wikipedia, Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron, dan keberulangan sifat kimia. Tabel juga terbagi menjadi empat blok: blok -s, -p, -d, dan -f. Secara umum, dalam satu periode (baris), di sebelah kiri bersifat logam, dan di sebelah kanan bersifat non-logam.
Baris pada tabel disebut periode, sedangkan kolom disebut golongan. Enam golongan (kolom) mempunyai nama selain nomor: contoh, unsur golongan 17 adalah halogen, dan golongan 18 adalah gas mulia. Tabel periodik dapat digunakan untuk menurunkan hubungan antara sifat-sifat unsur, dan memperkirakan sifat unsur baru yang belum ditemukan atau disintesis. Tabel periodik memberikan kerangka kerja untuk melakukan analisis perilaku kimia, dan banyak digunakan dalam bidang kimia dan ilmu lainnya.
Meskipun ada para pendahulunya, tabel periodik Dmitri Mendeleev adalah yang paling dipercaya, dalam publikasinya, pada tahun 1869, sebagai tabel periodik yang pertama kali diakui secara luas. Ia mengembangkan tabelnya untuk menggambarkan tren periodik berdasarkan sifat-sifat unsur-unsur yang telah diketahui.
Mendeleev juga memperkirakan beberapa sifat unsur-unsur yang belum diketahui yang akan mengisi ruang kosong dalam tabel tersebut. Sebagian besar prediksinya terbukti benar ketika unsur-unsur tersebut terungkap di kemudian hari. Tabel periodik Mendeleev telah dikembangkan dan dilengkapi dengan penemuan atau sintesis unsur-unsur baru dan pengembangan model teoretis baru untuk menjelaskan perilaku kimia.
Seluruh unsur dari nomor atom 1 (hidrogen) hingga 118 (oganesson) telah ditemukan atau disintesis, dengan penambahan terbaru (nihonium, moscovium, tennessine, dan oganesson) yang dikonfirmasi oleh International Union of Pure and Applied Chemistry (IUPAC) pada tanggal 30 Desember 2015 dan secara resmi diberi nama pada tanggal 28 November 2016: mereka menyelesaikan tujuh baris pertama Tabel periodik. Sembilan puluh empat unsur pertama terdapat secara alami, meskipun beberapa ditemukan dalam jumlah renik dan disintesis dalam laboratorium sebelum ditemukan di alam.
Unsur-unsur mulai nomor atom 95 hingga 118 adalah unsur sintetis yang dibuat di laboratorium. Bukti menunjukkan bahwa unsur-unsur nomor 95 s/d 100 sekali ditemukan di alam, tetapi saat ini tidak dijumpai lagi. Sintesis unsur dengan nomor atom yang lebih besar masih terus dikembangkan. Sejumlah radionuklida sintetis atau unsur yang berada di alam telah diproduksi di laboratorium.
Tabel periodik standar memberikan informasi dasar mengenai suatu unsur. Ada juga cara lain untuk menampilkan unsur-unsur kimia dengan memuat keterangan lebih atau dari persepektif yang berbeda.
Masing-masing unsur memiliki nomor atom unik yang menunjukkan jumlah proton dalam intinya. Sebagian besar unsur memiliki jumlah netron yang berbeda untuk atom yang berbeda. Hal semacam ini dikenal sebagai isotop. Sebagai contoh, karbon memiliki tiga isotop alami: semua atom tersebut memiliki enam proton dan sebagian besarnya memiliki enam netron juga, tetapi sekitar satu persen mempunyai tujuh netron, dan sebagian renik mempunyai delapan netron. Isotop tidak disajikan terpisah dalam tabel periodik. Mereka selalu dikelompokkan bersama sebagai unsur tunggal. Massa atom unsur yang tidak memiliki isotop stabil diambil dari isotop yang paling stabil, dituliskan di dalam kurung.
Beberapa presentasi memasukkan unsur nol. yaitu unsur yang tersusun hanya dari netron saja. Misalnya dalam Kimia Antariksa.
Dalam tabel periodik standar, unsur disusun menurut kenaikan nomor atom (jumlah proton dalam inti atom). Baris (periode) baru dimulai saat kulit elektron baru mempunyai elektron pertamanya. Kolom (golongan) ditentukan berdasarkan konfigurasi elektron; unsur-unsur yang memiliki kesamaan jumlah elektron dalam subkulit tertentu berada dalam kolom yang sama (contoh: oksigen dan selenium berada di kolom yang sama karena keduanya mempunyai empat elektron pada subkulit-p terluarnya).
Unsur-unsur dengan kesamaan sifat kimia biasanya jatuh ke dalam golongan yang sama pada tabel periodik, meskipun dalam blok-f, dan beberapa ditemukan di blok-d, unsur-unsur dalam periode yang sama cenderung memiliki kesamaan sifat kimia. Oleh karena itu, relatif mudah untuk memperkirakan sifat kimia suatu unsur jika diketahui sifat unsur-unsur di sekelilingnya.
Hingga tahun 2016, terdapat 118 unsur yang telah dikonfirmasi pada tabel periodik, meliputi unsur 1 (hidrogen) hingga 118 (oganesson), dengan penambahan terbaru (nihonium, moscovium, tennessine, dan oganesson) yang dikonfirmasi oleh International Union of Pure and Applied Chemistry (IUPAC) pada tanggal 30 Desember 2015 dan secara resmi diberi nama pada tanggal 28 November 2016: mereka menyelesaikan tujuh baris pertama Tabel periodik.
Sebanyak 94 unsur terdapat secara alami; sisanya 20 unsur dari amerisium hingga kopernisium dan flerovium serta livermorium, hanya ada jika disintesis di laboratorium. Dari 94 unsur alami, 84 adalah primordial (unsur purba). Sepuluh lainnya muncul jika ada peluruhan dari unsur primordial. Tidak ada unsur yang lebih berat daripada einsteinium (unsur 99) yang ditemui dalam jumlah besar dan bentuknya murni. Bahkan astatin (unsur 85); fransium (unsur 87) hanya terdeteksi dalam bentuk emisi cahaya dari jumlah mikroskopis (300.000 atom).